Exufiber käytännössä
Haavaa ympäröivän ihon kunto parani ja diabeetikoiden jalkahaavojen koko pieneni tutkimuksessa 21 potilaalla, joiden hoidossa käytettiin Exufiber®-sidosta.
Avoin, ei-vertaileva, postkliininen monikeskustutkimus geeliytyvien kuitusidosten tehosta ja turvallisuudesta diabeetikoiden jalkahaavojen hoidossa.
Chadwick, P., McCardle, J. Journal of Wound Care 2016; 25(4):290-300.
- Diabeetikoiden jalkahaavojen hoito on hankalaa.
- Huonossa hoidossa oleva diabetes lisää jalkahaavojen ja jalkojen amputaation riskiä.
- Sidosten valinta on tärkeä osa diabeetikoiden jalkahaavojen hoitoa.
- Diabeetikoiden jalkahaavat on yhdistetty lisääntyneiden hoitokustannusten ohella henkilökohtaiseen, sosiaaliseen ja taloudelliseen kuormitukseen.
- Muiden kroonisten haavojen tapaan myös diabeetikoiden jalkahaavat voivat erittää runsaasti, mikä altistaa niitä ympäröivän ihon maseraatiolle.
Tavoitteet
Tutkimuksen tavoitteena oli arvioida geeliytyvän Exufiber-kuitusidoksen tehoa ja turvallisuutta diabeetikoiden jalkahaavojen hoidossa.
Menetelmät
- Tutkimus oli avoin ei-vertaileva monikeskustutkimus.
- Mukaan otettiin sekä osastolla hoidettavia että avohoitopotilaita.
Ensisijainen tavoite:
- Arvioida Exufiber-sidoksen tehoa ja turvallisuutta diabeetikoiden jalkahaavojen hoidossa.
- Tutkimuksessa määritettiin tavoitteen mukaiset arviointiparametrit, joiden avulla seurattiin haavaa ympäröivän ihon kuntoa (muutoksia verrattiin tutkimuksen alkuarviointiin). Näitä parametreja olivat maseraatio, punoitus/ärsytys, ihottuma/ekseema, rakkulat, dermatiitti, ihon kuoriutuminen, haavan reunojen vauriot ja tuotteen hajoaminen iholla.
Toissijaiset tavoitteet:
- Sidokseen liittyvän kivun arviointi (100 mm:n kipujanalla, VAS).
- Haavan kunnon arviointi (koon ja paranemisvaiheen muutoksissa mitattuna).
- Terveydenhuollon ammattilaisen / potilaan mielipide testattavasta tuotteesta.
- Testattavan tuotteen tekninen toimivuus (poiston jälkeisissä sidoksen jäämissä ja haavaeritteen hallinnassa mitattuna).
- Tutkimukseen otettiin mukaan myös useammista haavoista kärsiviä potilaita, mutta varsinaisena tutkimuskohteena oli aina vain yksi haava.
- Jokainen potilas sai hoitoa paikallisten kliinisten rutiinien mukaisesti. Kaikkien sidosten käytössä noudatettiin valmistajan ohjeita.
- Potilaat olivat mukana tutkimuksessa, kunnes heidän haavansa parani kokonaan, hoidettava haava kuivui (jolloin testattava tuote ei enää soveltunut käyttöön) tai 12 viikon tutkimusjakson ajan.
- Potilaiden tila arvioitiin tutkimuksen alussa ja uudelleen viikoilla 1, 2, 4, 6, 8 ja 12.
- Sidokset vaihdettiin paikallisten kliinisten rutiinien mukaisesti (yleensä 3 kertaa viikossa) sidoksen imettyä itsensä täyteen tai haavan kunnon ja sijainnin mukaan. Sidosten vaihdot käyntien välillä sallittiin.
- Jokaisella arviointikäynnillä tarkkailtiin seuraavia muuttujia:
- haavan koko, tilavuus (mittaus Pictzar-ohjelmalla) ja sen syvimmän kohdan syvyys (mittaus vanupuikolla) – mittaukset tehtiin joka neljäs viikko ja lisäksi viikolla 6
- haavapohjan ulkonäkö
- haavaa ympäröivän ihon kunto
- tuotteen tekninen toimivuus
- haavaeritteen määrä ja tyyppi
- haavan puhdistuksen tarve
- haittatapahtumat/-vaikutukset
- kipu (ennen toissijaisen sidoksen poistamista sekä testattavan tuotteen poistamista ennen, sen aikana ja sen jälkeen) – osalla potilaista kivun arviointi ei ollut mahdollista neuropatian vuoksi
- infektion merkit.
Tulokset
- Tutkimukseen osallistui 21 potilasta kahdesta keskuksesta.
- Kaikki tutkimuksen potilaat (joiden hoitoon testattava tuote sopi) olivat valkoihoisia miehiä, joilla oli aktiivinen diabeetikon jalkahaava. Potilaiden keski-ikä oli 59,9 vuotta.
Ympäröivän ihon kunto
- Tutkimuksen alussa 6 potilaalla (28,6 %) haavaa ympäröivä iho oli terve/ehjä. Määrä lisääntyi 14 potilaaseen (66,7 %) viimeiseen käyntiin mennessä.
- Niiden potilaiden prosenttiosuus, joilla oli tiettyjä merkkejä ympäröivän ihon huonosta kunnosta, pieneni tai pysyi nollassa useimpien merkkien kohdalla tutkimuksen alusta viimeiseen käyntiin.
- Tuotteen hajoamista iholla ei havaittu.
Haavaerite
- Haavaeritteen määrä laski tasaisesti koko tutkimuksen ajan. Tutkimuksen alussa haavaeritettä esiintyi kaikilla potilailla, mutta viikolla 12 sitä ei esiintynyt 33,3 prosentilla potilaista.
- Haavaerite oli useimmiten heraista koko tutkimuksen ajan.
Kipu
- Kiputasot olivat erittäin matalia koko tutkimuksen ajan. (Osalla potilaista kivun arviointi ei ollut mahdollista neuropatian tai haavan paranemisen vuoksi.)
Haavan kunto
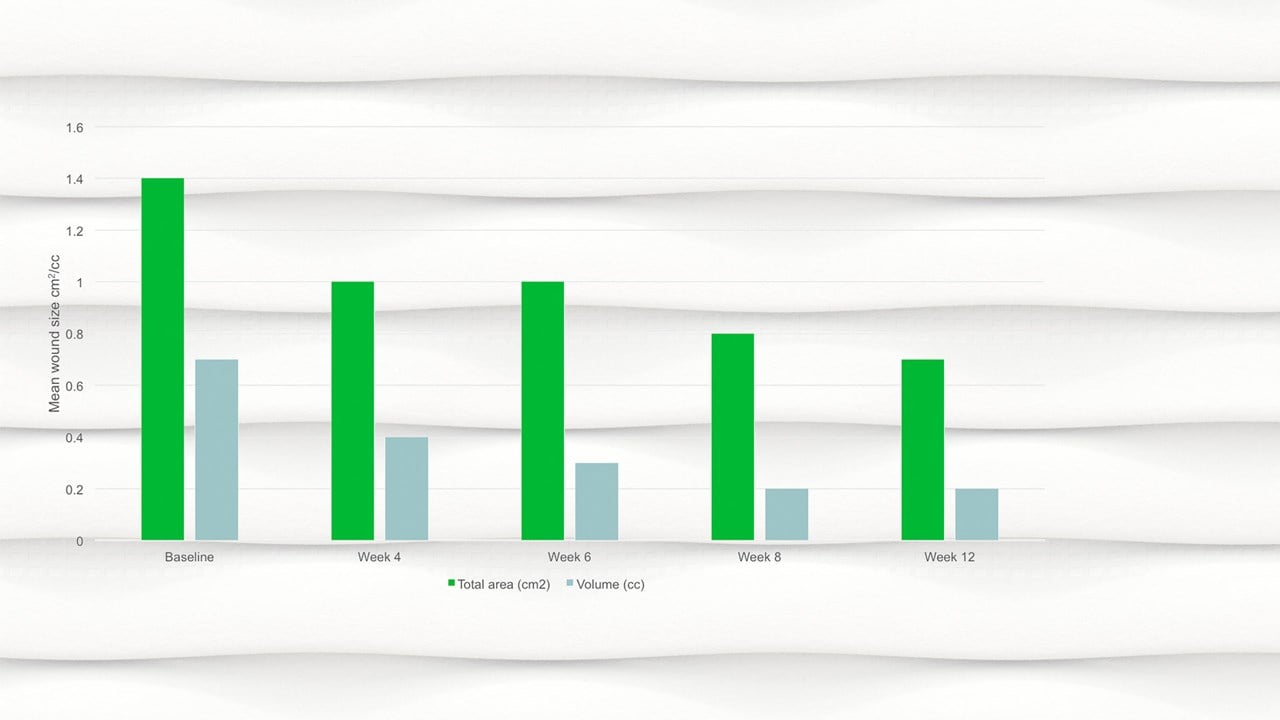
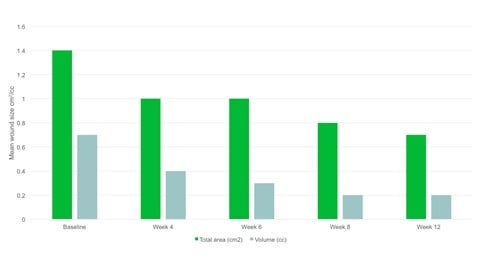
- Viikkoon 12 mennessä haavan keskimääräinen koko oli puolittunut tutkimuksen alusta keskimäärin 0,7 cm2.
- Haavan koko (p = 0,094) ja haavan tilavuus (p = 0,0056) pienenivät merkitsevästi tutkimuksen alusta viimeiseen käyntiin.
- Keskimääräinen epiteelikudoksen määrä kasvoi ja granulaatiokudoksen määrä väheni hieman tutkimuksen aikana. Elinkelvottoman kudoksen prosentuaalinen määrä pysyi vähäisenä koko tutkimuksen ajan.
- Parantuneiden haavojen määrä lisääntyi: viikolla 1 parantuneita haavoja oli yksi (4,8 %) ja viikolla 12 viisi (23,8 %).
Infektion merkit
Kliinisiä merkkejä infektiosta esiintyi vähän koko tutkimuksen ajan.
Tutkijoiden/hoitajien arviot
Tutkittavana oleva sidos sai hyvät arviot helposta asettamisesta ja poistamisesta, vähäisestä kiinnittymisestä haavapohjaan ja terveeseen ehjään ihoon poistamisen yhteydessä, joustavuudesta, mukautuvuudesta, haavaeritteen imukyvystä, katteen ja veren pidätyskyvystä ja yleisestä käyttökokemuksesta.
Potilaiden arviot
Tutkittavana oleva sidos sai hyvät arviot vähäisestä ahdistuksesta sidoksen vaihdon yhteydessä, liikkumisen helppoudesta, sidoksen paikallaan pysymisestä, pistämättömyydestä ja polttamattomuudesta sekä mukavuudesta käytön aikana.
Tutkimuksen aikana ei tehty ilmoituksia haittatapahtumista/-vaikutuksista, joiden olisi arvioitu liittyvän tutkittavan tuotteen käyttöön.
Johtopäätökset
- Tutkimustulokset osoittivat, että tutkittu sidos vähentää haavaa ympäröivän ihon vaurioitumista ja sidoksen vaihtoon liittyvää kipua.
- Vaikka useimmat haavat eivät parantuneet tutkimuksen aikana, niiden tila koheni, kun kudostyyppi ja haavan koon merkittävä pieneneminen otetaan huomioon.
- Sidoksen tekninen toimivuus haavaeritteen pidätys- ja imukyvyn suhteen osoitettiin.
- Tuotteen turvallisuudesta kertoo niiden potilaiden osuuden kasvu, joilla haavaa ympäröivä iho oli terve/ehjä, sekä se, että tuotteeseen liittyviä haittatapahtumia/-vaikutuksia ei esiintynyt.









